据披露,目前有超过15种不同的COVID-19候选疫苗正在世界各地进行人体测试,其中一些疫苗准备开始大规模的、最后阶段的研究,以证明它们是否真的有效。目前,来自国药集团中国生物的新冠灭活疫苗,以及阿斯利康与牛津大学合作的重组腺病毒疫苗——AZD1222都已经进入三期临床试验。
昨日,辉瑞与其德国合作伙伴BioNTech合作研制的mRNA的新冠病毒疫苗——BNT162b1也传来了新进展:在对45人进行的初步测试中,它可以提供能够阻断新冠病毒的中和抗体,防止感染。接受两次疫苗接种后,接受10 µg和30 µg剂量疫苗的志愿者体内新冠病毒中和抗体滴度分别达到康复患者血清水平的1.8和2.8倍,结果令人鼓舞。

(图:试验分别在欧美两地开展)
一项正在进行的美国1/2期安慰剂对照、观察者盲法临床试验中,45名年龄在18-55岁之间的健康受试者,成为了评估表达SARS-CoV-2受体结合结构域(RBD)的RNA候选疫苗(BNT162b1)的对象。BNT162b1是一款靶向刺突蛋白RBD的mRNA疫苗。它可以编码按照天然构象折叠的三聚体RBD。

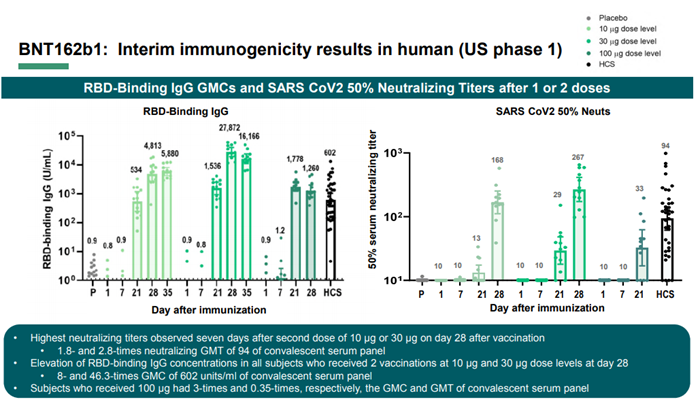
在28天(相隔21天接种第2剂),所有注射了10µg或30µg BNT162b1的受试者,产生了强力免疫反应。这些志愿者在第二次接种疫苗后第7天,血液中与RBD结合的IgG抗体水平达到峰值,抗体的几何平均水平(GMC)分别为4813单位/毫升,和27872单位/毫升。它们是从COVID-19康复患者中获得的38个血清样本中抗体平均水平的分别8倍和46.3倍之高。
结果显示,所有接受10次或30次BNT162b1的受试者均获得了抗SARS-CoV-2中和抗体,其几何平均滴度(GMTs)分别为168和267,分别为恢复期血清组GMT值的1.8倍和2.8倍。
不良反应方面,副作用主要是典型的注射部位疼痛和发热。在接受第二次疫苗注射后,8.3%接受10 µg剂量的志愿者和75.0%接受30 µg剂量的支援者出现≥38.0℃的发烧。试验中未出现严重不良反应。

该报告已提交在medRxiv预印本服务器上发表,但尚未经过同行评审。由于其他潜在的疫苗仍处于早期测试阶段,辉瑞计划在今年夏天开展大规模研究,但目前还不能确定哪种疫苗最好。
研究人员没有按照最初测试的最高剂量(单次100 µg剂量)注射第二次,而是坚持使用低剂量(10µg)和中剂量(30 µg)。高剂量(单次100 µg剂量)的注射引起更多的注射反应,但没有明显的额外效益。
BNT162b1是两家公司目前在临床试验中检验的4款mRNA疫苗之一。作为一款候选药物它仍在临床研究中,目前还没有批准在世界各地投入使用。
后续,辉瑞和BioNTech将持续跟进接受注射志愿者们体内的T细胞反应,根据后续超过6个月的跟进评估疫苗的安全性和免疫性反应。辉瑞和BioNTech还计划在7月下旬开始一项大型的全球2/3期试验,等待批准,试验将包括多达3万名健康参与者。
据悉,BioNTech也已经与复星医药达成合作协议,在中国进行这些疫苗的临床开发和推广。如果正在进行的研究成功,候选疫苗获得监管部门的批准,这些公司预计到2020年底生产1亿剂疫苗,到2021年底可能生产超过12亿剂。
编译/前瞻经济学人APP资讯组
参考来源:https://medicalxpress.com/news/2020-07-pfizer-early-vaccine-results.html
https://investors.biontech.de/news-releases/news-release-details/pfizer-and-biontech-announce-early-positive-data-ongoing-phase
https://investors.biontech.de/static-files/c4feb567-e564-40e5-a9cf-538892af1c04
https://www.medrxiv.org/content/10.1101/2020.06.30.20142570v1
品牌、内容合作请点这里:寻求合作 ››


 让您成为更懂趋势的人
让您成为更懂趋势的人
想看更多前瞻的文章?扫描右侧二维码,还可以获得以下福利:

下载APP

关注微信号


扫一扫下载APP
与资深行业研究员/经济学家互动交流让您成为更懂趋势的人
违法和不良信息举报电话:400-068-7188 举报邮箱:service@qianzhan.com 在线反馈/投诉 中国互联网联合辟谣平台
Copyright © 1998-2024 深圳前瞻资讯股份有限公司 All rights reserved. 粤ICP备11021828号-2 增值电信业务经营许可证:粤B2-20130734