


之江生物:公司新冠检测试剂盒可有效检出Omicron病毒
11月28日,之江生物微信公众号发布消息称,之江生物已上市的新型冠状病毒2019-nCoV核酸检测试剂盒,是针对病毒的ORF1ab、N、E三个靶基因进行特征性识别检测,与目前流行的变异株均进行了生物信息分析和对比验证,结果证实:之江生物已上市新型冠状病毒2019-nCoV核酸检测试剂盒,不会出现脱靶和漏检的情况。
全球首款皮下注射PD-L1恩沃利单抗在中国获批上市
25日,NMPA批准了皮下注射PD-L1抗体恩沃利单抗用于标准治疗失败的MSI-H/dMMR晚期结直肠癌、胃癌及其它实体瘤。该产品由思路迪医药、康宁杰瑞制药与先声药业三方共同合作开发,是目前全球首个获批的皮下注射给药的PD-(L)1抗体。

国内
第六批全国药品集采即将开标:胰岛素首进国采
第六批全国药品集采即将开标。根据国家组织药品联合采购办公室此前发布的《全国药品集中采购文件(胰岛素专项)(GY-YD2021-3)》,此次药品集采的申报信息时间是11月26日。从公开资料来看,这是胰岛素首次进入国采,也是生物药首次进入国采。
国家药监局药审中心公开征求《罕见疾病药物临床研究统计学指导原则(征求意见稿)》意见
为了鼓励制药企业研发罕见病治疗药物,提高临床研发效率和质量,药审中心组织起草了《罕见疾病药物临床研究统计学指导原则(征求意见稿)》,现公开征求意见。征求意见时限为自发布之日(11月26日)起1个月。
胰岛素国家集采结果公布:拟中选产品45个
26日,国家医保局在上海进行第六批国家组织药品集中带量采购工作,此次是对胰岛素的专项采购。根据3.2万家医疗机构提出的需求量计算,胰岛素集采需求量约2亿支,涉及金额约170亿元,事关全国1千万使用胰岛素患者。第六批国家胰岛素药品集采公布拟中选产品45个,药品平均降价47.67%。
开标在即!45个药品带量采购报价
22日,广东省药品交易中心发布《关于开展广东联盟阿莫西林等45个药品集团带量采购线上报价工作的通知》,企业报价时间已经确定,为11月24日上午9:00时至12:00时止。
双通道药店遴选标准来了!下月执行
23日,江西省医保局印发《江西省双通道谈判药品管理暂行办法》,并明确自2021年12月1日起实施。《办法》指出,双通道药品实行定点医疗机构、定点责任医师、定点零售药店的“双通道三定管理”,并在全省范围内互认。
国外
FDA宣布对新冠疫情采取的新行动
FDA宣布对新冠疫情采取的新行动:11 月 22 日,FDA 批准了三种非处方 (OTC) COVID-19 抗原诊断测试,用于 14 岁或 14 岁或以上的人使用自行收集的鼻拭子样本或 2 岁或以上的人在成人收集鼻拭子样本。11月18日,FDA批准了注射用盐酸万古霉素的缩略新药申请,用于治疗由耐甲氧西林(耐β-内酰胺类)葡萄球菌敏感菌株引起的严重或重症感染。
韩国发布部分修改药品禁忌成分规定的行政通知
韩国食品药品管理局在部分修改《药品禁用成分等规定》(食品药品安全部通报第2021-72号)中,添加了新的组合禁忌症、某些年龄组的禁忌症和妊娠禁忌症,以确保正确使用药物。

国内
美康生物:拟出资5亿元参设医药大健康产业基金
25日电,美康生物发布公告称,公司拟与启夏资本等共同发起设立生物医药大健康股权投资合伙企业,投资方向以生物医药医疗大健康产业为主。基金规模7亿元,其中美康生物认缴出资5亿元,其他有限合伙人合计认缴出资2亿元,基金期限8年。
德展健康作价4.26亿元向华创国信转让信托受益权
25日,德展健康发布公告称,为加快资金回流,公司拟以信托受益权转让的方式,对持有的4亿份信托单位进行全部处置退出,公司与华创国信签署了《信托受益权转让协议》,将公司2018年10月与中融信托签署的信托合同项下的4亿份信托单位所对应之信托受益权转让给华创国信,转让价款总额4.26亿元。
海翔药业:聘请陈芬儿院士为公司首席科学家
11月28日,海翔药业发布公告称,为加快推进公司科技创新和产品升级,公司决定聘请陈芬儿院士为公司首席科学家,任期5年,并与陈芬儿院士签署了《首席科学家聘任协议》。陈芬儿院士是中国工程院院士,复旦大学教授、博士生导师,长期从事合成药物化学和制药工程研究,在医药制造、精细有机化工及工程化方面取得了非凡成就。
振东制药董事、总裁马士锋因个人原因辞职
近日,振东制药发布公告,马士锋因个人原因,申请辞去公司董事、总裁、董事会薪酬与考核委员会委员、董事会审计委员会委员的职务。辞去上述职务后,马士锋不再担任公司任何职务。
国外
因疫情,FDA在外国监管和新药现场考察方面存在困难
在 疫情一年半后,FDA 已开始调整其国内药品生产检查的步伐。一份报告显示,尽管如此,该机构仍在努力应对外国工厂的监管,越来越多的新药申请面临延误。2021 年 4 月至 9 月期间,监管机构仅进行了 37 次外国药品检查、3 次外国动物药品检查、4 次外国医疗器械检查和 2 次外国生物制剂检查。
欧洲药管局建议批准辉瑞新冠疫苗用于5至11岁儿童
25日,欧洲药品管理局发表公报,建议欧盟委员会批准美国辉瑞公司和德国生物新技术公司联合开发的新冠疫苗用于5至11岁儿童。此前,该疫苗已获批用于成人和12岁以上青少年。
辉瑞新冠口服药Paxlovid每疗程529美元
近日,Pfizer发布公告称,美国政府已经以52.9亿美元的价格订购了1000万疗程的口服抗新冠病毒药物Paxlovid,前提是该药物已获监管机构批准。这意味着Paxlovid的售价为一个疗程529美元。
赛诺菲斥资 1.8 亿美元解决庞贝病特许权使用费纠纷
随着赛诺菲的庞贝病特许经营权推动了其在罕见疾病领域的增长,该公司已就一种关键药物的许可达成了 1.8 亿美元的和解协议。台湾公司证监会最近表示,赛诺菲旗下Genzyme公司已同意斥资 1.8 亿美元解决与美国和欧洲庞贝许可证相关的特许权使用费的分歧。
诺和、赛诺菲、礼来在中国胰岛素降价中受冲击
在胰岛素发现一百周年之际,中国决定对糖尿病疗法进行一轮降价。结果,外国公司诺和诺德、赛诺菲和礼来在关键市场上受到了打击。从明年开始,诺和、赛诺菲和礼来将放弃他们在市场上的主导地位,因为他们的降价幅度不足以与中国公司竞争。

国内
首付款1亿元!康诺亚生物抗TSLP单抗授权石药集团
22日,康诺亚宣布其全资附属公司康诺亚与石药集团全资附属公司上海津曼特生物科技有限公司就康诺亚创新药物CM326在中重度哮喘和慢性阻塞性肺病等呼吸系统疾病独家授权开发及商业化正式签订协议。此笔交易首付款和里程碑付款总计达1.7亿元人民币。
赛诺菲与百度合作开发mRNA疫苗 牵手Owkin布局AI制药
近日,赛诺菲达成了两项合作,和Owkin合作开发针对4种特定类型癌症的新疗法;获得百度mRNA序列设计算法,用于疫苗和治疗产品的设计。
罗氏及控股公司FMI与迪安诊断终止现有合作
11月27日,罗氏制药中国传播部相关负责人向赛柏蓝确认,罗氏及控股公司Foundation Medicine(FMI)和中国合作伙伴迪安诊断共同决定,终止现有合作。
国外
逾10亿美元助力开发治疗NASH的RNAi疗法,葛兰素史克达成合作
23日,Arrowhead Pharmaceuticals宣布,已经与GSK达成合作协议,共同开发和推广其在研RNAi疗法ARO-HSD,用于治疗非酒精性脂肪性肝炎。根据协议,Arrowhead将获得1.2亿美元前期付款,并有资格获得超过10亿美元的开发和商业化里程碑付款。GSK将获得ARO-HSD在大中华区之外的开发和商业化权益。
逾9亿美元开发创新DNA疫苗 再生元达成合作
23日,Nykode Therapeutics宣布,已与再生元达成一项授权合作协议,合作发现、开发和商业化5款新型DNA疫苗,以治疗癌症与预防传染病。根据协议条款,Nykode将获得3000万美元的预付款和2000万美元的股权投资。此外,Nykode将有资格获得超过8.75亿美元的里程碑付款,与未来潜在商业化产品销售的分级特许权使用费。
Xencor与Zenas就在研抗体obexelimab达成合作
日前,Xencor宣布,Zenas BioPharma已经从Xencor获得了在研抗体obexelimab的全球开发、生产和商业化权利。Obexelimab是一种新型双功能抗体,它同时靶向抑制B细胞活性的FcγRIIb和B细胞表达的CD19抗原,用于治疗自身免疫性疾病。

国内
国产新冠特效药有望12月底前获批附条件上市
22日,由清华大学、深圳市第三人民医院和腾盛博药合作研发的新冠药物BRII-196和BRII-198联合用药临床Ⅲ期已揭盲,给药组在治疗28天后实现零死亡,对照组8例死亡,详细结果会在近期对外公布。这也是目前我国进展最快的抗体药物,有望12月底前获得批准附条件上市。与欧美已获批紧急使用的新冠抗体药相比,该药是唯一进行了变异株感染者治疗效果评估并获得数据的。
安图生物糖类抗原CA15-3检测试剂盒获得医疗器械注册证
23日,安图生物发布公告称,公司于近日收到河南省药监局颁发的糖类抗原CA15-3检测试剂盒的《医疗器械注册证》,用于体外定量检测人血清中糖类抗原CA15-3的含量。
百济神州百悦泽®在欧盟获批治疗成人华氏巨球蛋白血症
24日,百济神州宣布,欧盟委员会批准百悦泽®用于治疗既往接受过至少一种治疗的华氏巨球蛋白血症成人患者,或作为不适合化疗免疫治疗WM患者的一线治疗方案。
武田抗病毒疗法Livtencity获得FDA批准上市
24日,FDA宣布,批准武田开发的抗病毒疗法Livtencity上市,用于治疗接受造血干细胞移植或实体器官移植后成人或12岁以上儿童患者的难治性巨细胞病毒感染。这是针对这一患者群体的首款获批疗法。
康宁杰瑞KN046联合化疗治疗晚期胰腺癌Ⅲ期临床申请获CDE批准
24日,康宁杰瑞PD-L1/CTLA-4双特异性抗体KN046联合白蛋白紫杉醇与吉西他滨治疗晚期胰腺癌的Ⅲ期注册临床研究申请获CDE批准。
国外
一次性基因疗法获FDA优先审评资格 治疗β地中海贫血
22日,bluebird bio宣布,FDA已授予基因疗法betibeglogene autotemcel的生物制品许可申请优先审评资格,用于治疗需要接受常规血红细胞输注的β地中海贫血患者。如果获得批准,这将是FDA批准的首款造血干细胞体外基因疗法。
CRISPR基因编辑改良 创新CAR-T疗法获FDA再生医学先进疗法认定
22日,CRISPR Therapeutics宣布FDA已授予CTX110再生医学先进疗法认定。CTX110是一款利用CRISPR基因编辑技术改造的同种异体CAR-T细胞疗法,用于治疗CD19阳性的B细胞恶性肿瘤患者。
GSK完整长效HIV疗法在华申报上市
25日,CDE官网显示,NMPA已受理GSK/ViiV Healthcare HIV药物卡替拉韦注射液和卡替拉韦钠片的上市申请。有望成为国内上市的首款完整长效HIV疗法,将使感染者用药天数由365天缩短至12天。
明德生物新冠抗原检测产品获得马来西亚和越南卫生部认证
25日,明德生物发布公告称,近日公司研制的新型冠状病毒抗原检测试剂盒取得马来西亚卫生部MDA认证,新型冠状病毒抗原快速检测试剂盒取得越南卫生部MOH认证。
驯鹿医疗CD19/CD22双靶点CAR-T细胞疗法获美国FDA孤儿药认定
11月26日, 驯鹿医疗宣布美国食品药品监督管理局孤儿药开发办公室已正式书面回函,授予公司自主研发的全人源抗CD19和CD22双靶点嵌合抗原受体自体T细胞注射液(CT120)孤儿药资格认定,用于治疗急性白血病。

国内
君实第二款新冠中和抗体获批临床
近日,君实生物发布公告,称JS026注射液临床试验申请获NMPA批准,用于新型冠状病毒肺的预防和治疗。
信达生物引进的SIRPα抗体在中国获批临床
22日,CDE公示显示,信达生物申报的IBI397获得一项临床试验默示许可,拟开发治疗晚期恶性肿瘤。
口服新冠药阿兹夫定:三期临床试验中 力争12月申请附条件上市
阿兹夫定是靶向RNA逆转录酶的抗艾滋病1类新药。针对新冠肺炎,在细胞水平和动物水平具有良好的抗新冠病毒活性,正在中国、巴西、俄罗斯开展III期临床试验。国内临床试验方面,已完成242例患者入组,正在协调增加郑州大学第一附属医院作为III期临床试验分中心,加速推进剩余患者入组,力争12月申请国内附条件批准上市。
针对乳腺癌!亿腾景昂在中国启动LAG-3疗法2期临床
中国药物临床试验登记与信息公示平台显示,亿腾景昂子公司亿佰康医药已在中国启动一项2期临床研究,以评价重组人源淋巴细胞激活基因-3融合蛋白注射液联合白蛋白紫杉醇,在激素受体阳性、人表皮生长因子受体2阴性的内分泌治疗进展的晚期乳腺癌患者中的安全性和疗效。
针对膀胱癌!凌腾医药卡妥索双抗1/2期试验完成首例患者给药
近日,凌腾医药宣布其在研抗体药物卡妥索双抗用于非肌层浸润性膀胱癌的1/2期临床试验完成首例患者给药。这是一项多中心临床研究,旨在观察卡妥索双抗对卡介苗治疗失败或不耐受的NMIBC患者的安全性与有效性。
国外
Arvinas/辉瑞公布“明星”PROTAC疗法最新临床结果
日前,Arvinas和辉瑞联合宣布,双方联合开发的PROTAC蛋白降解疗法ARV-471的最新1期临床结果将在12月上旬举行的圣安东尼奥乳腺癌研讨会上公布。在34名可以评估临床获益的患者中,临床获益率为41%。截至数据截止日,34名患者中6名患者仍在接受治疗,其中两名患者已经接受治疗超过16个月。
双特异性抗体治疗难治性HER2阳性乳腺癌临床结果积极
日前,Zymeworks宣布,其靶向HER2的双特异性抗体zanidatamab与化疗联用,在治疗接受过多种前期治疗的难治性HER2阳性乳腺癌患者的1期临床试验中,表现出令人鼓舞和持久的抗癌活性。试验结果显示,在16名可以评估应答的患者中,组合疗法达到37.5%的客观缓解率和81.3%的疾病控制率。
mRNA呼吸道合胞病毒疫苗启动全球性临床试验
近日,Moderna宣布,候选疫苗mRNA-1345的2/3期临床试验已完成首例患者给药,用于预防呼吸道合胞病毒感染。
尚健生物CD38/CD47双抗在美获批临床
22日,尚健生物宣布,其自主研发的全球首个靶向CD38/CD47双抗SG2501获FDA批准开展临床研究。CD47是一种广泛表达于多种癌细胞表面的糖蛋白,通过与肿瘤吞噬细胞表面SIRPα连接释放“别吃我”信号,阻止巨噬细胞吞噬作用。

阿里健康2022财年中期业绩:净亏损2.3亿元 上年同期利润2.8亿元
24日晚间,阿里健康发布2022财年中期业绩公告。数据显示,阿里健康上半年营收93.6亿元,同比增长31%;上半年净亏损2.318亿元,上年同期利润2.834亿元;上半年毛利率20%,上年同期26%。
李氏大药厂公布2021年前三季度业绩 实现收益约9.52亿港元
李氏大药厂公布2021年前三季度业绩,实现收益约9.52亿港元,同比增长6.5%;毛利约6.35亿港元,同比增长10.3%;毛利率为66.7%,较去年同期的64.4%上升2.3个百分点,主要源于回顾季度内若干专利产品的材料采购成本改善。

艺妙神州完成D轮战略融资,加快CAR-T产品开发
近日,北京艺妙神州医药科技有限公司顺利完成数亿元D轮战略融资。本轮融资由国寿大健康基金领投,广发乾和、水木深安、亚杰天使等机构共同参与。本次融资资金将用于加快临床推进步伐和商业化生产开发,推动公司的IM19成为首个国产自主开发的细胞药物。
泛因医学完成3000万元PreA轮战略融资
2021年11月25日,临床免疫诊疗企业泛因医学宣布完成了3000万人民币的PreA轮融资。本轮投资是由康圣环球参与发起,瑞江投资管理的瑞江康圣基金领投,跟投方包括火花创投和长江源通基金投资。泛因医学曾获得国内首个血液肿瘤MRD欧盟CE注册证,本轮资金将主要用于血液肿瘤MRD产品的推广及临床新产品的研发。

生物医药产业链全景梳理:疫苗、诊断试剂领域近两年增速快,单抗领域附加值高
生物医药产业链的上游为基础研究的开展,通常是由独立医学实验室,即第三方检测中心完成,有部分医院亦设有独立实验室,可承担一部分医药外包的项目。中游为生物医药制造,包含疫苗、血液制品、诊断试剂以及单克隆抗体领域。下游为消费终端,分别为医疗机构(含医院、基层医疗卫生机构、专业公共卫生机构)以及医药零售终端(包括实体药店以及电商平台)。

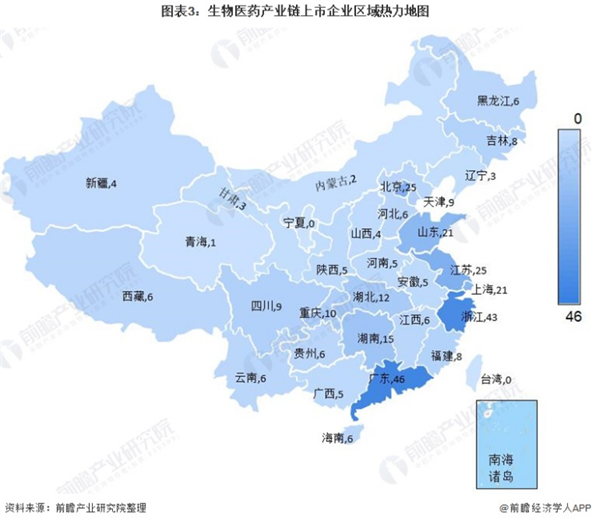
生物医药产业链区域热力图:广东地区上市企业集聚效应强,北京,长三角地区协同发展
从生物医药产业链上市企业的区域分布情况来看,中国生物医药产业链上市企业分布在广东、浙江、江苏、上海、北京等地区,且规模较大,广东省产业集聚效应较为明显,长三角地区一体化趋势明显,政策扶持生物医药行业协同发展。

从学术到产业,更多定制化产业周刊(全球产业舆情监测、前沿技术情报追踪、产融政策权威解读、产业招商精准线索),敬请拨打400-068-7188。同时前瞻产业研究院提供产业研究、产业咨询、产业大数据、IPO募投可研、招股说明书撰写等解决方案。
品牌、内容合作请点这里:寻求合作 ››


 让您成为更懂趋势的人
让您成为更懂趋势的人
想看更多前瞻的文章?扫描右侧二维码,还可以获得以下福利:

下载APP

关注微信号


扫一扫下载APP
与资深行业研究员/经济学家互动交流让您成为更懂趋势的人
违法和不良信息举报电话:400-068-7188 举报邮箱:service@qianzhan.com 在线反馈/投诉 中国互联网联合辟谣平台
Copyright © 1998-2025 深圳前瞻资讯股份有限公司 All rights reserved. 粤ICP备11021828号-2 增值电信业务经营许可证:粤B2-20130734