


阿斯利康中国区业务重大调整 呼吸与消化及自体免疫业务合并
15日,阿斯利康中国决定合并呼吸及自体免疫事业部、消化与呼吸雾化事业部,成立呼吸、消化及自体免疫事业部;新事业部将由现任阿斯利康中国副总裁、呼吸及自体免疫事业部负责人林骁带领。该全新架构调整从2月15日起执行。
Remix与杨森达成超10亿美元合作,开辟靶向RNA新模式
17日,Remix宣布与强生旗下杨森达成一项研发合作,利用Remix的REMaster药物发现平台,开发调节RNA加工的小分子治疗药物。根据协议条款,Remix将获得4500万美元的前期付款和研究资金,并可能获得临床前、临床期、和商业化里程碑付款、以及任何由此产生产品未来的分级特许权使用费,潜在总金额可能超过10亿美元。

2022年第一批议价药品(自费药)挂网采购通知发布
15日,上海阳光医药采购网发布《关于公布2022年第一批议价药品(自费药)挂网采购的通知》,涉及恒瑞医药普瑞巴林缓释片、科伦药业醋酸钠林格注射液、齐鲁制药注射用重组人促卵泡激素等42个品规。
安徽省药监局发布药品质量抽检结果 837批次产品全部符合规定
15日,安徽省药监局发布公告称,全省各级药品监管部门和药品检验机构对本行政区域药品生产、经营企业和使用单位的药品质量的抽查检验结果如下:本期抽验信息共涉及191个抽样单位,258个药品生产企业的837批次产品,检验结果全部符合规定。
第七批国采企业开始申报 共涉及208个品规
17日,上海阳光医药采购网发布《关于开展第七批国家组织药品集中采购相关药品信息填报工作的通知》,自2022年2月18日起,联合采购办公室开展第七批国家组织药品集中采购相关药品信息填报工作。此次国采共涉及208个品规,包括阿法替尼口服常释剂型、阿立哌唑口腔崩解片、昂丹司琼注射剂等。
上海公布2021年12月份超“黄线”幅度较大采购品种挂网名单
16日,上海阳光医药采购网发布《关于公布2021年12月份药品挂网公开议价超“黄线”幅度较大采购品种名单的通知》,涉及胞磷胆碱注射液、注射用二羟丙茶碱等20个品规的药品。

新型冠状病毒肺炎抗病毒新药临床试验技术指导原则(试行)发布
17日,CDE官网显示,为指导新型冠状病毒肺炎抗病毒药物的科学研发和评价,提供可供参考的技术标准,CDE制定了《新型冠状病毒肺炎抗病毒新药临床试验技术指导原则(试行)》。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》要求,经NMPA审查同意,现予发布,自发布之日起施行。
中国拟启动新冠疫苗加强针“混打”方案 智飞和康希诺入选
18日,新冠疫苗加强针“混打”方案或即将出台。目标人群可选择智飞龙科马的重组蛋白疫苗或康希诺的腺病毒载体疫苗中的一种,免费开展1剂次序贯加强针。
mRNA新冠疫苗在临床前研究中表现出良好的稳定性和免疫原性
12日,瑞科生物公布了其子公司武汉瑞科吉生物科技有限公司冻干剂型mRNA新冠肺炎疫苗的临床前数据。瑞科吉生物的冻干剂型mRNA-LNP新冠肺炎疫苗采用LNP递送系统,应用自主开发的冷冻干燥技术实现了4℃和25℃条件下的制剂稳定性。该疫苗可在常规冷链条件下贮存与运输,极大地提高了疫苗的可及性。此外,数据表明冻干工艺不影响该疫苗的关键理化指标、生物学活性和免疫原性。
Moderna计划设立4家子公司扩展亚洲市场
近日,Moderna宣布,公司计划在马来西亚、新加坡以及中国台湾省、中国香港特别行政区开设4家子公司,扩展亚洲市场将帮助公司增强COVID-19疫苗以及未来其他潜在mRNA疗法的制造能力和销售业绩。

企业合作
美国ACC累计向九安医疗美国子公司支付货款29.5亿元
17日,九安医疗发布公告称,根据合同主要内容中的交货安排,截至美国当地时间15日,公司美国子公司已经就iHealth试剂盒产品向合同对手方交货共计1.77亿人份。美国ACC已经累计向公司美国子公司支付货款4.65亿美元,上述货款已于美国时间16日全部到账,约合人民币29.5亿元。上述合同的履行对2022年度营业收入和营业利润将产生积极影响。
西湖欧米与焕一生物强强联手
2022年2月,西湖欧米与焕一生物签署了合作备忘录。双方将联合自身优势,从蛋白质组和代谢组学出发,结合AI+系统免疫分析技术,针对肿瘤和免疫疾病相关领域,共同推进临床多组学诊断产品研发,并向药企提供以生物标记物及靶点为导向的新药研发服务,为患者提供AI赋能的精准诊疗解决方案。
上海谊众与百洋医药达成战略合作
近日,上海谊众药业股份有限公司与青岛百洋医药股份有限公司在青岛签署合作协议,双方将就上海谊众旗下肿瘤创新药物“注射用紫杉醇聚合物胶束”紫晟®的商业化开展合作,共同推进国产肿瘤创新药物可及性,惠及国内众多肿瘤患者。
天吉生物与高瑞药业和博瑞生物达成合作
近日,苏州天马医药集团天吉生物制药有限公司与高瑞药业(北京)科技有限公司和博瑞生物医药(苏州)股份有限公司正式达成多肽偶联药物BGC0222的技术转让协议。资料显示,BGC0222是基于药品SN38开发的1类新药,属于一种新型的基于高分子载体的肿瘤靶向配体偶联药物。适应症包括结肠癌、胰腺癌、乳腺癌、小细胞肺癌、胃癌及脑胶质瘤等实体瘤。
企业收购
Equillium收购Bioniz Therapeutics
16日,Equillium宣布收购Bioniz Therapeutics。通过此次收购,Equillium将收获Bioniz的BNZ-1和BNZ-2以及包括BNZ-3在内的发现平台。
公司成立/注销
康众医疗对外投资设立全资子公司
16日,康众医疗发布公告称,公司拟以自有资金不超过1500万美元设立全资子公司 COMPASS INNOVATION SINGAPORE PTE. LTD.(暂定名)。该全资子公司设立后将被纳入康众医疗合并报表范围内,合并报表范围将发生变更。
步长制药注销全资子公司中欣顺发
16日,步长制药发布公告称,公司根据目前的实际经营情况及后续业务发展规划,为优化资源配置及组织结构,降低管理成本,提高运营管理效率,决定对其全资子公司中欣顺发予以注销。
人事变动
FDA换帅
15日,Robert Califf以50票对46票的微弱优势被美国参议院确认为FDA的新负责人。据悉,Califf曾于2016年2月至2017年1月担任FDA专员。在此前的391天里,FDA由Janet Woodcock临时执掌,如今,Robert Califf正式走马上任。
华润双鹤董事韩跃伟辞职
14日,华润双鹤发布公告称,因工作安排原因,韩跃伟申请辞去公司第九届董事会董事、专门委员会委员职务,辞职申请自送达董事会之日起生效。
奥精医疗更换公司董事会秘书 聘任高级管理人员
14日晚间,奥精医疗发布公告称,因公司内部工作调整变动,于秀荣不再担任公司董事会秘书职务,自董事会审议通过之日起生效,卸任后于秀荣仍担任公司财务负责人职务。此外,公司聘任仇志烨为公司董事会秘书,仇志烨现任公司副总经理职务,分管研发及市场工作。
诺禾致源独立董事史本军辞职
15日,诺禾致源发布公告称,史本军因个人原因申请辞去公司第二届董事会独立董事职务及董事会下设专门委员会相应职务,辞职后不再担任公司任何职务,其辞职在新任独立董事补选后生效。

葛兰素史克Benlysta在华获批新适应症
近日,葛兰素史克宣布,NMPA已批准Benlysta用于治疗正在接受标准护理的活动性狼疮性肾炎成人患者。此次最新批准,使Benlysta成为中国第一个也是唯一一个被批准用于治疗SLE的LN的生物制剂。
信达生物与驯鹿医疗BCMA CAR-T获美国FDA授予认定
14日,信达生物与驯鹿医疗共同宣布FDA孤儿药开发办公室已正式书面回函,授予两家公司共同开发的全人源自体B细胞成熟抗原嵌合抗原受体自体T细胞注射液孤儿药资格认定,用于治疗复发/难治性多发性骨髓瘤。
华兰生物控股子公司四价流感病毒裂解疫苗获批上市
华兰生物2月14日晚间公告,公司控股子公司华兰生物疫苗股份有限公司取得四价流感病毒裂解疫苗(儿童剂型)的药品注册证书。公司称,四价流感病毒裂解疫苗(儿童剂型)可正式生产和销售,将对公司2022年度经营业绩产生积极影响。
嘉和生物英夫利西单抗即将获批上市
17日,NMPA官网显示,嘉和生物的英夫利西单抗生物类似药上市申请进度「在审批」阶段,有望在近日获得批准。如若获批,这将是国产第3款英夫利西单抗生物类似药。
百时美施贵宝CAR-T疗法获FDA优先审评资格
17日,BMS宣布,美国FDA已授予靶向CD19的CAR-T细胞疗法Breyanzi的补充生物制品许可申请优先审评资格,以扩大其目前的适应症,用于治疗一线治疗失败后的复发/难治性大B细胞淋巴瘤成人患者。
以明生物抗LILRB4抗体IO-202获FDA快速通道资格
2月17日,以明生物(Immune-Onc Therapeutics)宣布在研抗LILRB4抗体IO-202获得美国FDA授予的快速通道资格,用于治疗复发或难治性急性髓系白血病(AML)。公开资料显示,IO-202是一款靶向LILRB4的潜在“first-in-class”髓系免疫检查点抑制剂,此前已经获得FDA授予的孤儿药资格,用于治疗AML。
治疗胆道癌!百济神州注射用ZW25拟纳入突破性治疗品种
17日,CDE官网公示,百济神州注射用ZW25拟纳入突破性治疗品种。注射用ZW25单药用于治疗既往接受系统化疗失败的HER2阳性的局部晚期不可切除或转移性胆道癌。公开资料显示,注射用ZW25是一款靶向HER2的双特异性抗体

单抗/双抗
信达PCSK9单抗3期临床达到终点
17日,信达生物宣布,公司自主研发的重组全人源抗前蛋白转化酶枯草溶菌素9单克隆抗体的两项中国关键注册临床研究——CREDIT-1研究(治疗非家族性高胆固醇血症合并高危/极高危心血管风险)和 CREDIT-4 研究(治疗非家族性高胆固醇血症和杂合子型家族性高胆固醇血症),均达到主要研究终点。
荣昌生物公布ADC维迪西妥单抗最新研究数据
17日,荣昌生物公布了其HER2靶向抗体偶联药物维迪西妥单抗联合疗法治疗局部晚期或转移性尿路上皮癌的最新临床进展。这是一项治疗局部晚期或转移性尿路上皮癌的1b/2期临床研究,最新数据显示,该药在所有患者中,研究者评估的客观缓解率为75%,一线治疗转移性尿路上皮癌患者的总体ORR为80%。研究表明,患者在不论治疗线数、HER2和PD-L1表达状态的情况下,均能从维迪西妥单抗和特瑞普利单抗的联合治疗中获益,而且ORR随HER2或PD-L1高表达而升高。值得一提的是,在HER2(3+)患者中的ORR高达100%。
无效!赛诺菲/再生元Dupixent治疗三期临床将停止
18日,再生元和赛诺菲宣布,根据预先指定的中期分析,评估Dupixent在慢性自发性荨麻疹患者中的3期试验将因无效而停止。Dupixent是由再生元的VelocImmune平台开发出来的首个针对IL-4Rα的全人源抗体,该药能够选择性地抑制关键性白介素4和白介素13信号通路,降低2型炎症的病理性反应,从机制上治疗2型炎症相关疾病,比如哮喘、慢性鼻窦炎伴鼻息肉病和特应性皮炎等。
Lonca在中国启动国际多中心III期临床
近日,中国药物临床试验登记与信息公示平台显示,Loncastuximab Tesirine在中国启动了国际多中心III期临床试验,这是一款靶向CD19的抗体偶联药物,针对复发或难治性弥漫大B细胞淋巴瘤患者。
安博生物CD70靶向ADC步入临床
15日,安博生物宣布,其公司为抗体偶联药物ARX305递交的IND申请已经获得美国FDA的许可。在多种肿瘤细胞和模型中,ARX305表现出良好的体外和体内效果,有望直接杀死过表达CD70的肿瘤,并改善肿瘤微环境。
先进疗法
传奇生物一项CAR-T疗法临床试验遭FDA叫停
近日,根据国外生物制药网站Fierce Pharma的报道,美国FDA通知传奇生物一项临床暂停,并将于3月11日前提供正式的临床暂停函。此次临床暂停涉及传奇生物的一款早期CAR-T细胞疗法。
Denali大分子递送技术有望挺进2/3期临床试验
日前,Denali Therapeutics宣布了在研酶替代疗法DNL310在一项正在进行的1/2期临床试验中获得的更新长期数据。DNL310是该公司使用酶转运载体技术开发的能够穿越血脑屏障的酶替代疗法,旨在治疗II型黏多糖贮积症的中枢神经系统和外周症状。基于迄今为止的临床期和临床前数据,Denali计划在今年上半年启动一项2/3期临床试验,旨在评估DNL310在MPS II患者中的疗效和安全性。
亘喜生物GC012F首次人体临床试验完成首批患者给药
18日,亘喜生物宣布全新开展了一项评估公司核心候选产品BCMA/CD19双靶点自体CAR-T细胞疗法GC012F,治疗B细胞非霍奇金淋巴瘤的临床试验,并已完成多名患者给药。
Arvinas公布雄激素受体PROTAC疗法最新结果
15日,Arvinas公布的最新数据显示,以雄激素受体为靶点的新型PROTAC蛋白降解剂bavdegalutamide,针对转移性去势抵抗性前列腺癌,继续提供抗肿瘤活性和患者获益的证据。这些数据表明,在46%肿瘤携带AR T878X/H875Y突变的患者中,bavdegalutamide使前列腺特异性抗原水平降低≥50%。基于这一结果,Arvinas计划在2022年年底之前启动一项关键性临床试验,评估bavdegalutamide治疗mCRPC患者的效果。
Nordic新型RSV疫苗获FDA突破性疗法认定
14日,Bavarian Nordic宣布,FDA已授予候选疫苗MVA-BN RSV突破性疗法认定,用于60岁或以上成人的主动免疫,以预防呼吸道合胞病毒引起的下呼吸道疾病。
Axcella Therapeutics多靶点口服药物获FDA快速通道资格
14日,Axcella Therapeutics宣布,FDA已授予AXA1125治疗伴肝纤维化非酒精性脂肪性肝炎的快速通道资格。AXA1125是一种多靶点口服候选药物,目前正在一项针对NASH患者的2b期临床试验中接受评估,预计在今年获得中期结果。
蔼睦医疗AM712临床申请获FDA批准
15日,蔼睦医疗宣布,FDA已批准其 AM712的临床开发新药研究申请。AM712 是一款新型双特异性生物分子,能够同时阻断血管内皮生长因子和血管生成素-2,治疗视网膜血管疾病。

益普生2021年销售额28.689亿欧元 同比增长10.7%
近日,益普生发布2021年业绩报告,总销售额为28.689亿欧元,与去年相比增长10.7%;其中,特殊护理业务销售额为26.433亿欧元,增长11.0%,CHC业务销售额为2.256亿欧元,增长7.1%。
万泰生物2021年净利同比增长197.83%
14日,万泰生物发布业绩快报,2021年公司实现营业收入57.5亿元,同比增长144.25%;实现利润总额23.21亿元,同比增长203.59%;实现归属于上市公司股东的净利润20.16亿元,同比增长197.83%;实现归属于上市公司股东的扣除非经常性损益的净利润19.4亿元,同比增长214.48%。
汇宇制药2021年净利润4.53亿元 同比增长31.96%
14日,汇宇制药披露业绩快报,公司实现营业总收入18.32万元,较上年增长34.26%;研发费用2.47亿元,较上年增长178.51%;实现营业利润4.87亿元,较上年同期增加22.37%;实现利润总额4.86亿元,较上年同期增加22.59%;实现归属于母公司所有者的净利润4.53亿元,较上年同期增加31.96%;实现归属于母公司所有者的扣除非经常性损益的净利润4.22亿元,较上年同期增加29.80%。

Ventus Therapeutics完成1.4亿美元C轮融资
近日,Ventus Therapeutics宣布完成1.4亿美元的C轮融资。获得的资金将用于支持加速其结构免疫学ReSOLVE平台的发展,以针对传统上认为“不可成药”的蛋白靶点开发药物,治疗免疫学、炎症和神经病学领域的广泛疾病。并通过自动化过程、扩展机器学习能力和构建更大的专有虚拟文库来增强平台性能。
Curevo获6000万美元A轮融资
日前,Curevo Vaccine宣布完成6000万美元的A轮融资。其先导项目CRV-101是一种用于预防带状疱疹的佐剂亚基疫苗,在1期临床试验中已经证明了其强大的免疫原性和耐受性。本轮融资获得的资金将用于推进这一疫苗的2b期临床试验。
Collegium以6.04亿美元收购BDSI
14日,Collegium公司宣布,已与BioDelivery Sciences达成最终协议,以每股5.6美元的现金收购后者,总金额高达6.04亿美元。Collegium预计2022年该收购可以产生7500万美元的协同效应。
天科雅完成超3亿元融资 开发免疫细胞药
近日,天科雅宣布完成超过3亿元的新一轮融资,融资将加速其免疫细胞产品的研发、产品线的拓展及支持公司核心产品的同时在中国和美国进行临床开发和商业化准备,以及招募和建立规模化的国际领先的团队。
SpliceBio获5000万欧元A轮融资
17日,SpliceBio宣布完成5000万欧元的A轮融资。融资获得资金将用于推动其基于蛋白剪接的主打在研基因疗法进入临床开发,用于治疗Stargardt病,并且扩展其研发管线,治疗目前尚无法治疗的遗传性疾病。
赛元生物完成近亿元融资
16日,赛元生物宣布完成近亿元新一轮融资,本轮融资由济峰资本领投,老股东昆仑资本超额跟投。融资将帮助公司提升研发能力和技术迭代创新,扩充具有国际性竞争力的研发产品管线,把即用型免疫细胞产品等推向临床。

证监会同意海创药业科创板IPO注册
15日,中国证监会官网显示,同意海创药业首次公开发行股票并在科创板上市的注册申请。此次IPO拟募资25.04亿元用于研发生产基地建设、创新药研发项目和发展储备资金。
康乐卫士拟申请北交所上市
15日,康乐卫士发布公告称,公司拟向不特定合格投资者公开发行股票并在北证所上市。本次拟发行股票数量不超过4,453万股,不高于发行后总股本的25%,发行底价为77.68元/股。
证监会同意普蕊斯、富士莱医药创业板IPO注册
16日,证监会同意普蕊斯和富士莱医药创业板首次公开发行股票注册。普蕊斯是一家提供临床试验现场管理服务的SMO企业,公司客户主要包括国内外制药公司、医疗器械公司等。富士莱医药主营原料药及中间体、保健品原料的研发、生产和销售,主要经营硫辛酸及衍生物,L-肌肽及衍生物和磷脂酰胆碱及衍生物三大系列产品。
华兰疫苗创业板上市,收涨超33%
18日,华兰疫苗在深交所创业板上市,公司证券代码为301207,首次公开发行后总股本为40,001万股。截至今日收盘,华兰疫苗报70.3元/股,涨幅23.59%,成交额17.04亿元,总市值281.21亿元。
歌礼在欧洲多个国家递交利托那韦上市许可申请
近日,歌礼制药有限公司宣布,通过欧洲代理商已向德国、法国、爱尔兰和英国递交了利托那韦(100毫克薄膜衣片)上市许可申请。其他包括在欧洲国家、北美国家和亚太国家的利托那韦的上市许可申请也预计将在近期递交。

全球生物医药行业专利技术周期
2010-2020年,全球生物医药行业专利申请人数量及专利申请量均呈现增长态势。2020年全球生物医药行业专利申请量及专利申请人数量分别为17968项和5820位。整体来看,全球生物医药技术处于成长期。
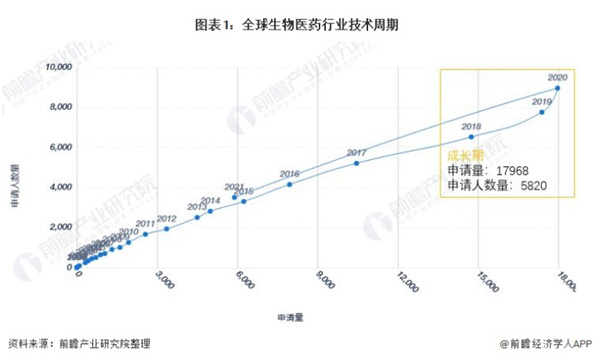
注:当前技术领域生命周期所处阶段通过专利申请量与专利申请人数量随时间的推移而变化来分析。
全球生物医药行业专利申请量及授权量
2010-2020年全球生物医药行业专利申请数量呈现逐年增长态势,2020年全球生物医药行业专利申请数量为17968项。
在专利授权方面,2010-2018年全球生物医药行业专利授权数量逐年增长,2019年开始出现下降趋势,2020年全球生物医药行业专利授权数量为5820项,授权比重为32.39%。
2021年1-10月,全球生物医药行业专利申请数量和专利授权数量分别为5890项和334项,授权比重为5.67%。截止2021年10月14日,全球生物医药行业专利申请数量10.5万项。

注:①专利授权率表明申请的有效率以及最终获得授权的提交申请成功率。
②统计说明:如果2012年专利申请在2014年获得授权,授予的专利将在2012年专利申请中显示。

从学术到产业,更多定制化产业周刊(全球产业舆情监测、前沿技术情报追踪、产融政策权威解读、产业招商精准线索),敬请拨打400-068-7188。同时前瞻产业研究院还提供产业大数据、产业研究、产业链咨询、产业图谱、产业规划、园区规划、产业招商引资、IPO募投可研、IPO业务与技术撰写、IPO工作底稿咨询等解决方案。
品牌、内容合作请点这里:寻求合作 ››


 让您成为更懂趋势的人
让您成为更懂趋势的人
想看更多前瞻的文章?扫描右侧二维码,还可以获得以下福利:

下载APP

关注微信号


扫一扫下载APP
与资深行业研究员/经济学家互动交流让您成为更懂趋势的人
违法和不良信息举报电话:400-068-7188 举报邮箱:service@qianzhan.com 在线反馈/投诉 中国互联网联合辟谣平台
Copyright © 1998-2026 深圳前瞻资讯股份有限公司 All rights reserved. 粤ICP备11021828号-2 增值电信业务经营许可证:粤B2-20130734